در نظام پیچیده و استراتژیک تجارت جهانی، صنعت داروسازی به عنوان یکی از پیشرانهای اصلی توسعه اقتصادی و نماد اقتدار علمی کشورها شناخته میشود. بازرگانان و تولیدکنندگانی که در سال ۱۴۰۴ قصد ورود به بازارهای بینالمللی را دارند، با محیطی روبرو هستند که در آن رعایت استانداردهای “روشهای خوب تولید” (GMP) و تسلط بر فرآیندهای رگولاتوری سازمان غذا و دارو (IFDA) نه تنها یک مزیت رقابتی، بلکه شرط بقا محسوب میشود.
گزارش تحلیلی «دریافت گواهی GMP و مجوز صادرات دارو ۱۴۰۴» با نگاهی به تحولات ژئوپلیتیک سالهای ۲۰۲۵ و ۲۰۲۶، از جمله بازگشت مکانیسم ماشه و فشارهای ارزی، نقشه راهی جامع برای دریافت گواهی GMP و اخذ مجوزهای صادراتی ترسیم میکند تا فعالان اقتصادی بتوانند با کمترین ریسک، محصولات سلامتمحور ایران را در تراز جهانی عرضه نمایند.
مبانی و فلسفه استانداردهای GMP در صنعت داروسازی نوین
استاندارد “روشهای خوب تولید” یا Good Manufacturing Practice که به اختصار GMP نامیده میشود، بخشی از سیستم مدیریت کیفیت است که تضمین میکند محصولات دارویی به طور مداوم و بر اساس استانداردهای کیفی متناسب با کاربرد مورد نظرشان و الزامات پروانه بازاریابی تولید و کنترل میشوند.1
هدف بنیادین GMP، به حداقل رساندن خطرات ذاتی در هر فرآیند تولید دارویی است که با آزمایش نهایی محصول قابل شناسایی نیستند. این خطرات عمدتاً شامل آلودگیهای متقاطع (Cross-contamination)، تداخلات محصولی (Mix-ups) و برچسبگذاری اشتباه میشوند.1 در دنیای داروسازی، هرگونه نقص در کیفیت میتواند مستقیماً جان انسانها را به خطر بیندازد، لذا GMP نه به عنوان یک مانع اداری، بلکه به عنوان یک میثاق اخلاقی و فنی میان تولیدکننده و مصرفکننده عمل میکند.3
بر اساس آخرین راهنماهای سازمان جهانی بهداشت (WHO) در سال ۲۰۲۵، مدیریت کیفیت در صنایع دارویی باید از مرحله طراحی ساختمان و انتخاب تجهیزات آغاز شده و تا دورافتادهترین نقاط زنجیره توزیع ادامه یابد.1 بازرسان رگولاتوری دیگر تنها به بررسی اسناد نهایی اکتفا نمیکنند، بلکه بر “فرهنگ کیفیت” در سازمان تأکید دارند، جایی که هر اپراتور خط تولید، خود را مسئول نهایی سلامت بیمار میداند.5 در سال ۱۴۰۴، با توجه به پیشرفتهای تکنولوژیک، استفاده از سیستمهای مانیتورینگ آنلاین و هوش مصنوعی در پایش فرآیندهای تولید به یکی از اجزای جداییناپذیر ارزیابیهای GMP تبدیل شده است.6

ارکان ده گانه GMP و اهمیت آنها در اعتبار رگولاتوری
برای دستیابی به سطح مطلوبی از انطباق با استانداردهای بینالمللی، بازرگانان و تولیدکنندگان باید بر ده رکن اساسی تمرکز کنند. این ارکان شامل نیروی انسانی آموزشدیده، فضا و تأسیسات مناسب، تجهیزات کالیبره شده، مواد اولیه تأیید شده، دستورالعملهای مکتوب (SOPs)، سوابق تولید بچ، سیستم کنترل کیفیت مستقل، شرایط انبارداری استاندارد، سیستم توزیع تحت کنترل و در نهایت، فرآیند رسیدگی به شکایات و بازخوانی محصول هستند.7
نکته کلیدی در اینجا “اعتبارسنجی” یا Validation است. تولیدکننده باید ثابت کند که هر مرحله بحرانی از فرآیند تولید، تحت شرایط تعریف شده، همواره محصولی با کیفیت یکسان به دست میدهد.9 در جدول زیر، مقایسهای میان الزامات کلیدی در حوزههای مختلف تولید بر اساس استانداردهای ۲۰۲۵ ارائه شده است:
| حوزه فعالیت | الزامات کلیدی GMP | اهمیت استراتژیک در صادرات |
| تأسیسات و ساختمان | جداسازی مناطق تولید، کنترل HVAC، سیستمهای آبساز (WFI) | جلوگیری از آلودگی متقاطع و تضمین استریلیته 7 |
| تجهیزات | استیل ضدزنگ ۳۱۶، کالیبراسیون دورهای، قابلیت شستشو (CIP/SIP) | حذف بقایای مواد قبلی و دقت در دوزبندی 10 |
| پرسنل | آموزشهای تخصصی، بهداشت فردی، مسئول فنی واجد شرایط | کاهش خطاهای انسانی به عنوان عامل اصلی نقص کیفیت 10 |
| مستندسازی | سوابق بچ (BPR)، دستورالعملهای استاندارد (SOP)، گزارشهای انحراف | ردیابی کامل محصول در صورت بروز عوارض ناخواسته 5 |
| کنترل کیفیت (QC) | آزمایشگاههای تأیید شده، متدهای ولید شده، نمونهبرداری علمی | سد نهایی قبل از ورود محصول به بازار مصرف 7 |
فرآیند اجرایی اخذ گواهی GMP از سازمان غذا و دارو ایران در سال ۱۴۰۴
در ایران، مرجع نهایی و قانونی صدور گواهی GMP، سازمان غذا و دارو (IFDA) است. برای بازرگانی که قصد صادرات دارو را دارد، اطمینان از اینکه واحد تولیدی دارای این گواهی است، اولین قدم محسوب میشود.10 فرآیند با ثبتنام در سامانه تیتک (TTAC) آغاز میگردد. شرکتها موظفند مستندات مربوط به پروانه بهرهبرداری، نقشه ساختمانها (Site Master File)، لیست تجهیزات و رزومه مسئول فنی خود را در این سامانه بارگذاری کنند.11
پس از بررسی اولیه مستندات، تیم بازرسی سازمان غذا و دارو جهت بازدید حضوری به واحد تولیدی اعزام میشوند. این بازرسیها در سال ۱۴۰۴ با سختگیری بیشتری نسبت به سالهای گذشته انجام میشود، چرا که ایران به دنبال کسب عضویت کامل در کنوانسیون بازرسی دارویی (PIC/S) است.8 بازرسان بر “جریان مواد” و “جریان پرسنل” تمرکز ویژهای دارند تا اطمینان حاصل کنند که هیچ تداخلی میان مواد اولیه، محصولات میانی و محصولات نهایی وجود ندارد.7
مراحل گامبهگام پس از بازرسی و رفع عدم انطباقها
در صورتی که در جریان بازرسی، مواردی از عدم انطباق (Observation) مشاهده شود، به شرکت فرصت داده میشود تا در یک بازه زمانی مشخص، اقدامات اصلاحی و پیشگیرانه (CAPA) خود را ارائه دهد.8 عدم انطباقها معمولاً به سه دسته “بحرانی” (Critical)، “عمده” (Major) و “جزئی” (Minor) تقسیم میشوند.6 وجود حتی یک عدم انطباق بحرانی میتواند منجر به توقف خط تولید و عدم صدور گواهی گردد.
پس از تأیید اقدامات اصلاحی توسط کارشناسان، گواهی GMP صادر میشود که معمولاً دارای اعتبار دو ساله است.10 بازرگانان باید توجه داشته باشند که این گواهی برای هر خط تولید به صورت مجزا صادر میشود؛ بنابراین داشتن گواهی برای خط تولید قرص به معنای مجاز بودن تولید شربت یا ویال در آن واحد نیست.13
تدوین پرونده فنی دارو (CTD)؛ استانداردی برای ثبت بینالمللی
یکی از بزرگترین چالشهای بازرگانان در صادرات دارو، آمادهسازی مستندات فنی مطابق با استانداردهای کشور مقصد است. فرمت CTD یا Common Technical Document که توسط ICH تعریف شده، اکنون زبان مشترک تمام سازمانهای رگولاتوری دنیا از جمله ایران است.14 تدوین یک CTD دقیق، نه تنها فرآیند ثبت محصول در کشور هدف را تسریع میکند، بلکه نشاندهنده حرفهای بودن شرکت صادرکننده است.
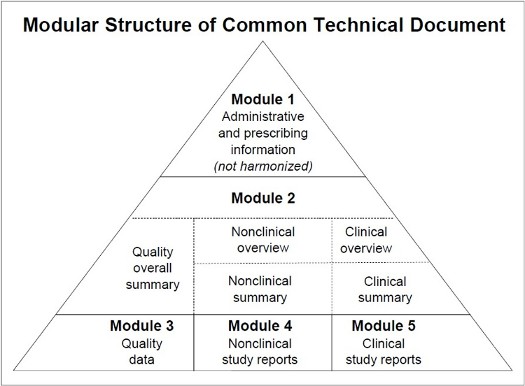
پرونده جامع دارویی شامل ۵ ماژول اصلی است که از اطلاعات اداری تا گزارشهای بالینی را پوشش میدهد.15 برای بازرگانان، تسلط بر محتویات این ماژولها جهت مذاکره با شرکای خارجی و ارائه مستندات لازم حیاتی است.
تحلیل ساختاری ماژولهای پنجگانه پرونده فنی
ماژول ۱ به اطلاعات اداری و منطقهای اختصاص دارد. این بخش شامل فرمهای درخواست، مجوزهای شرکت، گواهی GMP، برچسبها و بروشورهای محصول است.15 ماژول ۲ شامل خلاصههای کلی از کیفیت، ایمنی و اثربخشی است که به ارزیابان اجازه میدهد به سرعت محتوای علمی پرونده را درک کنند.15
ماژول ۳، فنیترین بخش پرونده است که به “کیفیت” اختصاص دارد. این ماژول به دو قسمت اصلی تقسیم میشود: ۱. بخش S (ماده موثره): شامل اطلاعات مربوط به سنتز، آنالیز، ناخالصیها و پایداری ماده اولیه دارویی (API) است.15 ۲. بخش P (محصول نهایی): شامل فرمولاسیون، فرآیند ساخت، اعتبارسنجی روشهای آنالیز، تستهای آزادسازی و مطالعات پایداری محصول نهایی در بستهبندی اصلی است.15
ماژولهای ۴ و ۵ به ترتیب شامل گزارشهای غیربالینی و بالینی هستند. برای داروهای ژنریک که بخش عمده صادرات ایران را تشکیل میدهند، در ماژول ۵ معمولاً مطالعات بیواکیوالانسی (Bioequivalence) ارائه میشود تا ثابت شود داروی ایرانی از نظر جذب و اثرگذاری با داروی برند اصلی (Reference) یکسان است.15
گواهیهای اختصاصی صادرات؛ CPP و FSC و نقش آنها در تجارت
پس از اینکه دارو در داخل کشور ثبت و تولید شد، بازرگان برای خروج محموله و ثبت آن در کشور مقصد به اسناد خاصی نیاز دارد. مهمترین این اسناد، “گواهی محصول دارویی” یا CPP (Certificate of Pharmaceutical Product) است.2 این گواهی که توسط سازمان غذا و دارو صادر میشود، بر اساس فرمت سازمان جهانی بهداشت (WHO) بوده و تأیید میکند که دارو در ایران دارای پروانه ساخت (Marketing Authorization) است و کارخانه تولیدکننده تحت نظارت مستمر GMP قرار دارد.2
گواهی دیگر، “گواهی فروش آزاد” یا FSC (Free Sale Certificate) است که نشان میدهد محصول بدون هیچ محدودیتی در بازار داخلی ایران به فروش میرسد.19 در بسیاری از کشورها، ارائه CPP یا FSC برای شروع فرآیند ثبت دارو الزامی است.
فرآیند درخواست و بازههای زمانی در سال ۱۴۰۴
در سال ۱۴۰۴، فرآیند صدور این گواهیها به صورت کاملاً الکترونیکی درآمده است. صادرکنندگان باید درخواست خود را در کارتابل مسئول فنی ثبت کنند. در صورت تکمیل مدارک، این گواهیها معمولاً ظرف ۳ تا ۵ روز کاری صادر میشوند.18 نکته مهم این است که برای صادرات داروهایی که در لیست کمبودهای کشوری قرار دارند، مجوز صادرات صادر نخواهد شد و اولویت همواره با تأمین نیاز داخلی است.21
| نوع گواهی | مرجع صدور | محتوای اصلی | کاربرد اصلی |
| CPP | سازمان غذا و دارو (IFDA) | تأیید ثبت دارو و انطباق با GMP طبق فرمت WHO | ثبت دارو در کشور مقصد 2 |
| FSC | سازمان غذا و دارو (IFDA) | تأیید اجازه فروش محصول در کشور مبدأ | اثبات ایمنی و مقبولیت کالا 20 |
| Health Certificate | معاونتهای غذا و دارو | تأیید سلامت فیزیکی و شیمیایی هر سری ساخت | ترخیص کالا از گمرک مقصد 19 |
| GMP Certificate | سازمان غذا و دارو (IFDA) | تأیید انطباق خطوط تولید با استانداردهای بینالمللی | پیشنیاز تمام فعالیتهای دارویی 10 |
چکلیست ضروری بازرگانان برای عملیات صادرات دارو
برای یک بازرگانی خارجی موفق در حوزه دارو، داشتن یک چکلیست دقیق برای هر محموله ضروری است. این فرآیند از تحقیق بازار آغاز شده و تا رفع تعهد ارزی ادامه مییابد.23 اولین گام، دریافت “کارت بازرگانی” معتبر و ثبت نام در سامانه جامع تجارت (NTSW) است.24 بازرگان باید اطمینان حاصل کند که کد HS محصول به درستی انتخاب شده است تا در محاسبات گمرکی دچار مشکل نشود.24
در مرحله بعد، انتخاب تولیدکننده دارای GMP معتبر و عقد قرارداد صادراتی اهمیت دارد. در سال ۱۴۰۴، صادرات داروهای تولید قراردادی (Contract Manufacturing) به شدت مورد توجه قرار گرفته است. در این مدل، شرکت بازرگانی میتواند دارویی را با نام تجاری خود در خط تولید یک کارخانه معتبر تولید کرده و صادر کند.13 این کار مستلزم اخذ “پروانه ساخت مخصوص صادرات” است که اجازه توزیع در داخل کشور را ندارد اما فرآیند صدور آن بسیار سریعتر از پروانههای عادی است.13
مدیریت زنجیره تأمین و لجستیک در شرایط سال ۲۰۲۶
با توجه به فشارهای بینالمللی و بازگشت برخی تحریمها در سال ۲۰۲۵، مدیریت لجستیک به یکی از پیچیدهترین بخشهای صادرات تبدیل شده است. هزینههای حملونقل و بیمه به دلیل شرایط ژئوپلیتیک تا ۵۰ درصد افزایش یافته و زمان ترانزیت کالا نیز طولانیتر شده است.26 بازرگانان باید از شرکتهای حملونقل متخصص در حوزه دارو استفاده کنند که دارای گواهی GDP (توزیع خوب) هستند.
استفاده از کانتینرهای یخچالی مجهز به دیتالاگر (Data Logger) برای داروهای حساس به دما الزامی است. هرگونه انحراف دمایی در طول مسیر میتواند منجر به تخریب مواد موثره دارو و رد محموله توسط خریدار خارجی گردد.27 همچنین، بازرگانان باید با اینکوترمز (Incoterms) به خوبی آشنا باشند؛ در حوزه دارو، استفاده از شرایطی مانند CIP یا CPT که در آن فروشنده مسئولیت و هزینه حمل تا مقصد را بر عهده میگیرد، برای جلب اعتماد مشتریان خارجی توصیه میشود.28
تحلیل چالشهای ارزی و مالی در افق ۱۴۰۴ و ۱۴۰۵
یکی از بزرگترین موانع در مسیر صادرات، موضوع نوسانات نرخ ارز و قوانین “رفع تعهد ارزی” است. در ژانویه ۲۰۲۶، نرخ ریال در برابر دلار به مرز ۱.۴ میلیون تومان رسیده است که این موضوع از یک سو باعث افزایش قیمت تمام شده مواد اولیه وارداتی (که ۷۰ درصد رشد داشته) و از سوی دیگر، جذابیت صادرات را افزایش داده است.26
بر اساس بخشنامههای بانک مرکزی برای سال ۱۴۰۴، صادرکنندگان دارو موظفند حداقل ۹۰ درصد از ارز حاصل از صادرات خود را به چرخه اقتصادی بازگردانند.30 روشهای رفع تعهد شامل فروش ارز در سامانه نیما، واردات در مقابل صادرات (خود یا غیر) و یا بازپرداخت بدهیهای ارزی است.31
تسهیلات و معافیتهای مالیاتی برای صادرکنندگان
دولت برای تشویق صادرات، معافیتهای مالیاتی خاصی را در نظر گرفته است. در صورتی که صادرکننده در مهلت قانونی (معمولاً ۶ ماه) تعهد ارزی خود را ایفا کند، مشمول مالیات با نرخ صفر خواهد بود.30 همچنین شرکتهای دانشبنیان در سال ۱۴۰۴ از تسهیلات ویژهای برخوردارند که شامل زمان طولانیتر برای رفع تعهد (تا ۱۵ ماه) و امکان استفاده از بخشی از ارز برای هزینههای تحقیق و توسعه بینالمللی است.30
نکته حیاتی برای بازرگانان در سال ۱۴۰۴، “تعهدنامه عدم استفاده از ارز حمایتی” است. اگر دارویی با مواد اولیه تهیه شده با ارز ترجیحی تولید شده باشد، صادرکننده باید مابهالتفاوت نرخ ارز را به حساب سازمان غذا و دارو واریز کند، در غیر این صورت صادرات آن محموله قاچاق محسوب میشود.19
تأثیر تحریمها و فشارهای بینالمللی بر تجارت دارو در سال ۲۰۲۵
سال ۲۰۲۵ با بازگشت سیاستهای “فشار حداکثری” و اعمال مجدد تحریمهای سازمان ملل تحت مکانیسم ماشه (Snapback)، محیط تجاری بسیار سختی را برای ایران رقم زده است.33 این تحریمها دسترسی ایران به ارز خارجی را محدود کرده و منجر به کمبود نقدینگی در میان واردکنندگان مواد اولیه شده است.26
اگرچه دارو و تجهیزات پزشکی به طور رسمی مشمول تحریمهای بشردوستانه نیستند، اما در عمل، تحریمهای بانکی فرآیند انتقال پول را بسیار دشوار و پرهزینه کرده است. بازرگانان اکنون مجبورند از کانالهای واسطه و صرافیهای غیررسمی استفاده کنند که ریسک تجارت را افزایش داده و شفافیت مالی را کاهش میدهد.29
راهکارهای مقابله با ریسکهای تحریمی برای بازرگانان
برای مقابله با این شرایط، فعالان حوزه دارو به سمت مدلهای “تهاتر” (Barter) و استفاده از ارزهای محلی در تجارت با کشورهایی مانند روسیه، چین و هند حرکت کردهاند.29 همچنین حضور در نمایشگاههای بینالمللی مانند CPhI چین یا دوفات دبی برای حفظ ارتباط با بازارهای جهانی حیاتی است، هرچند چالشهای سیاسی گاهی منجر به لغو پاویونهای ایران میشود.35
پیشنهاد میشود بازرگانان در سال ۱۴۰۴ بر صادرات “خدمات فنی و مهندسی دارویی” و “انتقال تکنولوژی” تمرکز کنند. با توجه به سطح بالای دانش فنی در ایران، راهاندازی خطوط تولید مشترک در کشورهای همسایه میتواند راهی برای دور زدن محدودیتهای حملونقل و بانکی باشد.
مطالعات پایداری و اهمیت مناطق اقلیمی در صادرات
یکی از جنبههای فنی که مستقیماً با گواهی GMP و پرونده CTD در ارتباط است، انجام مطالعات پایداری (Stability Studies) مطابق با شرایط اقلیمی کشور مقصد است. سازمان جهانی بهداشت جهان را به ۵ منطقه اقلیمی تقسیم کرده است. ایران در منطقه IVa قرار دارد، اما اگر قصد صادرات به برزیل یا سنگاپور را دارید، باید پایداری محصول خود را در شرایط منطقه IVb اثبات کنید.36
شرایط تست برای مناطق مختلف به شرح زیر است:
| منطقه اقلیمی | نوع آب و هوا | دمای تست طولانیمدت | رطوبت نسبی (RH) |
| Zone I | معتدل | ۲۱ درجه سانتیگراد | ۴۵ درصد |
| Zone II | نیمهگرمسیری و مدیترانهای | ۲۵ درجه سانتیگراد | ۶۰ درصد 36 |
| Zone III | گرم و خشک | ۳۰ درجه سانتیگراد | ۳۵ درصد |
| Zone IVa | گرم و مرطوب (مانند اکثر نقاط ایران) | ۳۰ درجه سانتیگراد | ۶۵ درصد 37 |
| Zone IVb | گرم و بسیار مرطوب | ۳۰ درجه سانتیگراد | ۷۵ درصد 37 |
انجام مطالعات پایداری تسریع شده (Accelerated) در دمای ۴۰ درجه و رطوبت ۷۵ درصد به مدت ۶ ماه، برای تمام داروها جهت پیشبینی عمر قفسهای الزامی است.27 بازرگانان باید این دادهها را از تولیدکننده مطالبه کرده و در پرونده صادراتی خود بگنجانند.
نتیجهگیری و چشمانداز استراتژیک برای فعالان اقتصادی
تجارت دارو در افق ۱۴۰۴، مسیری است که در آن تخصص فنی با هوشمندی بازرگانی گره خورده است. دریافت گواهی GMP دیگر یک برچسب ساده نیست، بلکه نمادی از کیفیت و اعتبار بینالمللی است که میتواند درهای بازارهای منطقه و فرامنطقهای را به روی محصولات ایرانی بگشاید. با وجود چالشهای ارزی، فشارهای تحریمی و پیچیدگیهای رگولاتوری، صنعت داروسازی ایران با اتکا به ظرفیتهای دانشبنیان و سامانههای نظارتی پیشرفته مانند تیتک، توانسته است در سال ۱۴۰۳ به صادراتی بیش از ۸۴ میلیون دلار دست یابد و این روند در سال ۱۴۰۴ با رشدی ۳۰ درصدی پیشبینی میشود.38
برای موفقیت پایدار، بازرگانان باید به سمت حرفهایگری در مستندسازی (CTD)، مدیریت دقیق زنجیره تأمین سرد و تسلط بر قوانین بانکی و ارزی حرکت کنند. اکنون زمان آن است که با بهرهگیری از فرصتهای برنامه هفتم توسعه، برند دارویی ایران را به عنوان جایگزینی باکیفیت و مقرونبهصرفه برای داروهای غربی در بازارهای در حال توسعه معرفی نماییم. آینده متعلق به کسانی است که کیفیت را نه یک هدف، بلکه مسیر حرکت خود قرار میدهند.
منابع
- Guidelines on Good Manufacturing Practices (WHO) – Health products policy and standards, accessed on February 4, 2026, https://www.who.int/teams/health-product-and-policy-standards/standards-and-specifications/norms-and-standards-for-pharmaceuticals/guidelines/production
- Good Manufacturing Practices (GMP) – Health products policy and standards, accessed on February 4, 2026, https://www.who.int/teams/health-product-policy-and-standards/standards-and-specifications/norms-and-standards/gmp
- Facts About the Current Good Manufacturing Practice (CGMP) – FDA, accessed on February 4, 2026, https://www.fda.gov/drugs/pharmaceutical-quality-resources/facts-about-current-good-manufacturing-practice-cgmp
- TRS 1060 – Annex 3: WHO good manufacturing practices for excipients used in pharmaceutical products – World Health Organization (WHO), accessed on February 4, 2026, https://www.who.int/publications/m/item/trs-1060—annex-3–who-good-manufacturing-practices-for-excipients-used-in-pharmaceutical-products
- گواهینامه GMP (اصول تولید خوب محصول) – ایزوسیستم, accessed on February 4, 2026, https://isosystem.org/certificate/gmp/
- Guidance on good manufacturing practice and good distribution practice: Questions and answers | European Medicines Agency (EMA), accessed on February 4, 2026, https://www.ema.europa.eu/en/human-regulatory-overview/research-development/compliance-research-development/good-manufacturing-practice/guidance-good-manufacturing-practice-good-distribution-practice-questions-answers
- Good manufacturing practices guide for drug products (GUI-0001) – Canada.ca, accessed on February 4, 2026, https://www.canada.ca/en/health-canada/services/drugs-health-products/compliance-enforcement/good-manufacturing-practices/guidance-documents/gmp-guidelines-0001/document.html
- گواهی GMP چیست؟ | مدارک و مراحل اخذ آن در ایران | – پی اس پی اکسپرس, accessed on February 4, 2026, https://pspexpress.com/fa/mag/gmp-certificate/
- چگونه گواهینامه GMP بگیریم؟ مراحل + قیمت – سایت ایزو, accessed on February 4, 2026, https://siteiso.com/%DA%86%DA%AF%D9%88%D9%86%D9%87-%DA%AF%D9%88%D8%A7%D9%87%DB%8C%D9%86%D8%A7%D9%85%D9%87-%D8%A7%DB%8C%D8%B2%D9%88-gmp-%D8%A8%DA%AF%DB%8C%D8%B1%DB%8C%D9%85%D8%9F/
- 9اصل استاندارد GMPو شرایط اخذ گواهینامه GMP سازمان غذاو دارو – شرکت ابراهیم, accessed on February 4, 2026, https://www.ebrahimco.com/blog/conditions-obtaining-gmp-certificate/
- کد irc چیست؟ مدارک – مراحل – نحوه استعلام (1404) – شرکت توسعه کیفیت, accessed on February 4, 2026, https://nhiso.com/what-is-the-meaning-of-irc-code/
- نحوه اخذ پروانه بهرهبرداری از سامانه TTAC چگونه است؟ | موسسه ثبتی و حقوقی تکسفیر, accessed on February 4, 2026, https://tregister.ir/%D9%86%D8%AD%D9%88%D9%87-%D8%A7%D8%AE%D8%B0-%D9%BE%D8%B1%D9%88%D8%A7%D9%86%D9%87-%D8%A8%D9%87%D8%B1%D9%87%D8%A8%D8%B1%D8%AF%D8%A7%D8%B1%DB%8C-%D8%A7%D8%B2-%D8%B3%D8%A7%D9%85%D8%A7%D9%86%D9%87/
- پروانه ساخت مخصوص صادارت – مدیریت غذا و دارو – دانشکده علوم پزشکی تربت جام, accessed on February 4, 2026, https://www.trjums.ac.ir/fda/fa/page/1477/%D9%BE%D8%B1%D9%88%D8%A7%D9%86%D9%87-%D8%B3%D8%A7%D8%AE%D8%AA-%D9%85%D8%AE%D8%B5%D9%88%D8%B5-%D8%B5%D8%A7%D8%AF%D8%A7%D8%B1%D8%AA
- CTD دارویی: ساختار، محتوا و چک لیست مورد نیاز – اکونوریس, accessed on February 4, 2026, https://econoris.ir/ctd-%D8%AF%D8%A7%D8%B1%D9%88%DB%8C%DB%8C-%D8%B3%D8%A7%D8%AE%D8%AA%D8%A7%D8%B1%D8%8C-%D9%85%D8%AD%D8%AA%D9%88%D8%A7-%D9%88-%DA%86%DA%A9-%D9%84%DB%8C%D8%B3%D8%AA-%D9%85%D9%88%D8%B1%D8%AF-%D9%86%DB%8C/
- نحوه تهیه ctd دارو و دارویی – 1404-11-10 – مبین فارمد افرا, accessed on February 4, 2026, https://mobinpharmed.ir/product/%D8%A2%D9%85%D9%88%D8%B2%D8%B4-ctd-%D9%85%D9%84%D8%B2%D9%88%D9%85%D8%A7%D8%AA/
- ctd دارویی چیست؟ | آموزش نحوه ساخت – سیب سبز سلامت, accessed on February 4, 2026, https://ghapple.com/blog/%D9%85%D9%82%D8%A7%D9%84%D8%A7%D8%AA-%D8%B3%D8%A7%DB%8C%D8%AA/P1282-ctd-%D8%AF%D8%A7%D8%B1%D9%88%DB%8C%DB%8C-%DA%86%DB%8C%D8%B3%D8%AA.html
- واردات دارو | مراحل ارسال دارو به ایران + مدارک لازم – شرکت بازرگانی راهکار تجارت پایا, accessed on February 4, 2026, https://rahkartejarat.com/importation/import-of-medicine/
- صدور گواهی صادرات FSC , CPP و GMP – ثبت بازرگان, accessed on February 4, 2026, https://sabtebazargan.com/%D8%B5%D8%AF%D9%88%D8%B1-%DA%AF%D9%88%D8%A7%D9%87%DB%8C-%D8%B5%D8%A7%D8%AF%D8%B1%D8%A7%D8%AA-fsc-cpp-%D9%88-gmp/
- گواهی بهداشت – معاونت غذا و دارو, accessed on February 4, 2026, https://fdo.tums.ac.ir/%DA%AF%D9%88%D8%A7%D9%87%DB%8C-%D8%A8%D9%87%D8%AF%D8%A7%D8%B4%D8%AA
- صدور گواهی صادرات FSC,CPP و GMP (فرآورده های طبیعی، سنتی و مکمل) – ثبت بازرگان, accessed on February 4, 2026, https://sabtebazargan.com/%D8%B5%D8%AF%D9%88%D8%B1-%DA%AF%D9%88%D8%A7%D9%87%DB%8C-%D8%B5%D8%A7%D8%AF%D8%B1%D8%A7%D8%AA-fsccpp-%D9%88-gmp-%D9%81%D8%B1%D8%A2%D9%88%D8%B1%D8%AF%D9%87-%D9%87%D8%A7%DB%8C-%D8%B7%D8%A8%DB%8C%D8%B9/
- صادرات و واردات دارویی ایران – سایت شرکت فراز فارمد, accessed on February 4, 2026, https://farazpharmed.ir/%D8%B5%D8%A7%D8%AF%D8%B1%D8%A7%D8%AA-%D9%88-%D9%88%D8%A7%D8%B1%D8%AF%D8%A7%D8%AA-%D8%AF%D8%A7%D8%B1%D9%88%DB%8C%DB%8C-%D8%A7%DB%8C%D8%B1%D8%A7%D9%86/
- دستورالعمل صادرات دارو – سندیکای صاحبان صنایع داروهای انسانی ایران, accessed on February 4, 2026, https://syndipharma.org/%D8%AF%D8%B3%D8%AA%D9%88%D8%B1%D8%A7%D9%84%D8%B9%D9%85%D9%84-%D8%B5%D8%A7%D8%AF%D8%B1%D8%A7%D8%AA-%D8%AF%D8%A7%D8%B1%D9%88/
- مراحل صادرات دارو + لیست داروهای صادراتی ایران, accessed on February 4, 2026, https://pourdanesh.com/%D9%85%D8%B1%D8%A7%D8%AD%D9%84-%D8%B5%D8%A7%D8%AF%D8%B1%D8%A7%D8%AA-%D8%AF%D8%A7%D8%B1%D9%88/
- مجوز های لازم برای صادرات و واردات کالا به ایران در سال 1404 – بازرگانی جولایی, accessed on February 4, 2026, https://joolaei.com/import-license-to-iran/
- به منظور صادرات ضابطه صدور پروانه تولید شیمیایی و فرآورده های بیولوژی, accessed on February 4, 2026, https://syndipharma.org/wp-content/uploads/2024/02/%D8%B6%D8%A7%D8%A8%D8%B7%D9%87-%D8%B5%D8%AF%D9%88%D8%B1-%D9%BE%D8%B1-1.pdf
- Iran drug and medical costs surge 70% after subsidy removal, accessed on February 4, 2026, https://www.iranintl.com/en/202511102505
- Annex 2 Stability testing of active pharmaceutical ingredients and finished pharmaceutical products, accessed on February 4, 2026, https://academy.gmp-compliance.org/guidemgr/files/WHO_TRS_953_ANNEX2.PDF
- step7 – پویش ملی صادرات, accessed on February 4, 2026, https://exportcampaign.com/step7/
- How US sanctions crippled lives of Iranians Trump says he wants to ‘help’ – Al Jazeera, accessed on February 4, 2026, https://www.aljazeera.com/news/2026/1/13/how-us-sanctions-crippled-lives-of-iranians-trump-says-he-wants-to-help
- آموزش رفع تعهد ارزی در صادرات | راهنمای کامل و سریع, accessed on February 4, 2026, https://jafari.business/%D8%A2%D9%85%D9%88%D8%B2%D8%B4-%D8%B1%D9%81%D8%B9-%D8%AA%D8%B9%D9%87%D8%AF-%D8%A7%D8%B1%D8%B2%DB%8C-%D8%AF%D8%B1-%D8%B5%D8%A7%D8%AF%D8%B1%D8%A7%D8%AA/
- دستورالعمل و ضوابط اجرایی رفع تعهد ارزی صادرکنندگان و برگشت ارز حاصل از صادرات کالا به چرخه اقتصادی کشور – اختبار, accessed on February 4, 2026, https://www.ekhtebar.ir/%D8%AF%D8%B3%D8%AA%D9%88%D8%B1%D8%A7%D9%84%D8%B9%D9%85%D9%84-%D9%88-%D8%B6%D9%88%D8%A7%D8%A8%D8%B7-%D8%A7%D8%AC%D8%B1%D8%A7%DB%8C%DB%8C-%D8%B1%D9%81%D8%B9-%D8%AA%D8%B9%D9%87%D8%AF-%D8%A7%D8%B1%D8%B2/
- رفع تعهدات ارزی – مشاوره حقوقی دینا, accessed on February 4, 2026, https://www.heyvalaw.com/web/articles/view/3488/%D8%B1%D9%81%D8%B9-%D8%AA%D8%B9%D9%87%D8%AF%D8%A7%D8%AA-%D8%A7%D8%B1%D8%B2%DB%8C.html
- Sanctions by the Numbers: 2025 Year in Review – CNAS, accessed on February 4, 2026, https://www.cnas.org/publications/reports/sanctions-by-the-numbers-2025-year-in-review
- Reimposition of UN-Mandated Sanctions Against Iran and Additional EU and UK Sanctions, accessed on February 4, 2026, https://www.cov.com/en/news-and-insights/insights/2025/10/reimposition-of-un-mandated-sanctions-against-iran-and-additional-eu-and-uk-sanctions
- فرصت طلایی صادرات دارویی بر باد رفت – تابناک | TABNAK, accessed on February 4, 2026, https://www.tabnak.ir/fa/news/1282308/%D9%81%D8%B1%D8%B5%D8%AA-%D8%B7%D9%84%D8%A7%DB%8C%DB%8C-%D8%B5%D8%A7%D8%AF%D8%B1%D8%A7%D8%AA-%D8%AF%D8%A7%D8%B1%D9%88%DB%8C%DB%8C-%D8%A8%D8%B1-%D8%A8%D8%A7%D8%AF-%D8%B1%D9%81%D8%AA
- Climatic Zones for Stability Studies | Climatic Zone Classification & Conditions | Pharmaguideline, accessed on February 4, 2026, https://www.pharmaguideline.com/2010/12/different-climatic-zones-for-stability.html
- Drug Stability: ICH versus Accelerated Predictive Stability Studies – PMC – NIH, accessed on February 4, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC9693625/
- صادرات داروهای ایرانی به ۴۰ کشور جهان | خبرگزاری بینالمللی شفقنا, accessed on February 4, 2026, https://fa.shafaqna.com/news/2031626/









